۱- آب آهک
طرز تهيه: ۵گرم اکسید کلسیم رادر۱۵۰میلی لیتر آب حل کنید. این محلول کدر، شیرآهک نامیده می شود. شیر آهک را با کاغذ صافی، صاف کنید. محلول صاف شده كه کاملاً شفاف است، آب آهک است.
كاربرد: شناسائي CO2 در هواي بازدمي وغيره
۲- محلول ید
طرز تهيه: ۲۵/۰ گرم ید جامد را در ۱۰۰سی سی الکل صنعتی حل می کنیم.
كاربرد: برای رنگ آمیزی سلول های پوششی دهان و تست نشاسته
۳- ايزوپروپيل الكل
طرز تهيه: از محلول۵۰٪ اين محلول تهيه مي شود
كاربرد: پاك كردن لنز عدسي ميكروسكوپ ها و تهيه محلول ها
۴- محلول تورنسل
طرز تهيه: یک گرم تورنسل را در کمی آب مقطر حل کرده و حجم آنرا به ۱۰۰سی سی می رسانیم.
كاربرد: معرف اسیدهاو بازها
۵- محلول هلیانتین(متیل اورانژ)
طرز تهيه: یک دهم گرم آن را در۱۰۰سی سی آب مقطرحل می کنیم
كاربرد: معرف اسید و بازها
۶- محلول نیترات نقره
طرز تهيه: یک گرم پودر نیترات نقره را در۱۰۰سی سی آب مقطرحل ميكنيم (نگهداری در شیشه های تیره )
كاربرد: برای شناخت نمک درعرق- آب معمولی و...
۷- چسب نشاسته
طرز تهيه: یک گرم نشاسته را در ۱۰۰سی سی آب مقطر ریخته و بهم می زنیم. سپس تا نقطه جوش حرارت داده و توسط کاغذ صافی، صاف می کنیم.
۸- آب ژاول
طرز تهيه: در یک شیشه مقداری پر منگنات پتاسیم ریخته و دهانه شیشه را به وسیله چوب پنبه دو سوراخه می بندیم. از یکی از سوراخ های آن بوسیله بورت که در آن اسید کلریدریک ریخته ایم اسید به پر منگنات اضافه می کنیم. از سوراخ دیگر چوپ پنبه لوله خمیده ای عبور می دهیم که سر دیگر آن در داخل سود سوز آور در داخل یک ارلن وارد شود. اسید با پر منگنات کلر آزاد کرده است و کلر با سود سوز آور ترکیب شده و هیپو کلرید سدیم می دهد.
كاربرد: برای از بین بردن ترکیبات داخل سلول
۹- محلول سولفات مس
طرز تهيه: یک گرم سولفات مس (کات کبود) را در ۱۰۰ سي سي آب مقطر حل می کنیم .
كاربرد: برای شناخت پروتئین
۱۰- سولفات مس بدون آب
طرز تهيه: حدود ۵ گرم سولفات مس آبی رنگ را در یک لوله آزمایش ریخته و روی شعله آن قدر حرارت می دهیم تا پودر آبی رنگ سفید شود .
۱۱- سولفات مس ۰۱/0%
طرز تهيه: ۱/۰گرم سولفات مس بدون آب رادريك ليتر آب حل كنيد
كاربرد: بعلت سمي بودن براي از كار انداختن آغازيان (سرعت حركت پارامسي راكم مي كند)
۱۲- محلول سود ۱۰٪
طرز تهيه: ۱۰ گرم سود جامد را با ترازو وزن کرده سپس آنرا در۱۰۰ميلي ليتر آب مقطر حل کرده و خوب بهم می زنیم .
كاربرد: برای تست پروتئین
۱۳- محلول پتاس ۵٪
طرز تهيه: ۲۵گرم پتاس جامد را وزن کرده و آن را در ۵۰۰ سی سی آب حل می کنیم.
كاربرد: برای جذب CO2 (طراحي آزمايش تأثير CO2 درفتوسنتز)
۱۴- اسید کلریدریک ۵/۰نرمال
طرز تهيه: ۵۰۰ سی سی آب مقطر را با ۵/۲۱ سی سی اسید کلریدریک تجاری مخلوط می کنیم.
۱۵- تهیه اسید کلریدریک یک نرمال
طرز تهيه: ۱۰۰سی سی آب مقطر را با۱/۸ سی سی اسید کلریدریک تجاری مخلوط می کنیم.
۱۶- محلول اسيد كلريدريك
طرز تهيه: ۱۸ ميلي ليتر اسید کلریدریک را در ۱۰۰ ميلي ليتر آب حل مي كنيم
كاربرد: بافت هاي گياهي
۱۷- محلول اسيد بوريك ۲ درصد
طرز تهيه: ۲گرم را اسيد بوريك در ۱۰۰ ميلي ليتر آب حل مي كنيم
۱۸ محلول كربنات سديم۵/۰ درصد
طرز تهيه: ۵/۰گرم كربنات سديم را در ۱۰۰ ميلي ليتر آب حل مي كنيم
۱۹- تهیه محلول بیکربنات سديم ۵درصد
طرز تهيه: ۵گرم بيكربنات سديم جامد را در ۱۰۰ سی سی آب حل می کنیم.
۲۰- تهیه محلول بیکربنات پتاسیم ۵درصد
طرز تهيه: ۵گرم بیکربنات پتاسیم را در ۱۰۰سی سی آب مقطر حل می کنیم.
كاربرد: برای دفع CO2
می پسندم 0 نمی پسندم 0
این مطلب در تاریخ: چهار شنبه 22 آذر 1391 ساعت: 17:9 منتشر شده است






























.gif)
.jpg)
.gif)








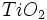 مصرفی در رنگسازی از نوع روتایل است. آناتاز را با حرارت دادن در 700-950 درجه سانتیگراد میتوان به روتایل تبدیل کرد.
مصرفی در رنگسازی از نوع روتایل است. آناتاز را با حرارت دادن در 700-950 درجه سانتیگراد میتوان به روتایل تبدیل کرد. 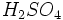 ،
، 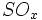 و بخار آب تولید میشود که وقتی وارد جو شوند، موجب آلودگی هوا خواهند شد. بنابراین استفاده از تصفیه کننده در کارخانهها ضروری است. از ضایعات دیگر این روش باز ، تولید اسید سولفوریک مصرف شده بدون برگشت آن به چرخه تولید میباشد.
و بخار آب تولید میشود که وقتی وارد جو شوند، موجب آلودگی هوا خواهند شد. بنابراین استفاده از تصفیه کننده در کارخانهها ضروری است. از ضایعات دیگر این روش باز ، تولید اسید سولفوریک مصرف شده بدون برگشت آن به چرخه تولید میباشد. 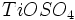
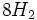
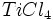 آن را تقطیر کرده و تتراکلرید تیتانیوم خالص را با اکسیژن هوا در شعلهای با دمای 1500 درجه سانتیگراد اکسید میکنند (واکنش سوختن). دراین فرایند دانههای بسیار ریز دیاکسید تیتانیوم و گاز کلر ایجاد میشود. کلر تولید شده دوباره وارد چرخه تولید میشود.
آن را تقطیر کرده و تتراکلرید تیتانیوم خالص را با اکسیژن هوا در شعلهای با دمای 1500 درجه سانتیگراد اکسید میکنند (واکنش سوختن). دراین فرایند دانههای بسیار ریز دیاکسید تیتانیوم و گاز کلر ایجاد میشود. کلر تولید شده دوباره وارد چرخه تولید میشود. 
 را ایجاد میکنند.
را ایجاد میکنند.




